

Riassunto
Il microbiota congiuntivale nel neonato presenta :
staph. aureus,H. influenzae,Neisserie, difteroidi.
nel bambino:
streptococchi viridanti,Staph. aureus,Pneumococchi.
Per raccogliere il secreto congiuntivale si usa un tampone sterile umido.
Con la spatolina di Kimura si può fare lo scraping congiuntivale. Per la
citologia coloriamo con Giemsa.
Cosa vediamo:cellule eosinofile e basofile sospetto di Chlamidia.Cellule
neutrofile sospetto di infezione batterica.
QUANDO A LIVELLO LOCALE LE IG A SECRETORIE SONO BASSE CIO' FA PENSARE A
CRONICIZZAZIONE. Si raccolgono le lacrime con capillare 10 ul all'angolo interno
e si pongono su vetrino già pronto con cellule infettate. Le Ig A servono a
valutare la reattività locale.Le lacrime si seminano direttamente su Lowenstein
Jensen per la ricerca dei micobatteri. Si seminano le lacrime direttamente su
BHI o tioglicollato brodo per la ricerca degli anaerobi. I parassiti della
retina sono le larve di Onchocerca volvulus diffuso in Africa equatoriale. Si
osservano al fondo oculare. Queste larve si osservano anche in sangue
periferico.Si osserva una grave iniezione della congiuntiva. Esiste la tipica
congiuntivite da Chlamidia trachomatis. Un altro parassita che si osserva al
fondo oculare è la Toxocara canis. Quando osserviamo una cheratite cioè una
secrezione della cornea si può colorare con inchiostro di china. Il trofozoita
si osserva con Lugol.Si vedono le propaggini di Acanthoameba. La cisti classica
di Acanthameba ha una aspetto a stella. L'edema palpebrale fa pensare a
Tripanosoma cruzii. Congiuntivite dei neonati:
batterica
allergica
virale:da adenovirus o herpes virus
chlamidia
La chlamidia nell'adulto può avere come causa la frequenza di piscine e da
lenti a contatto infette. Lo scraping (grattamento) congiuntivale fornisce
campioni che se hanno molte cellule ( buona cellularità) sono idonei
all'osservazione . Il dosaggio delle Ig A nel siero è importante per la
prognosi della infezione. Lo scraping congiuntivale è un prelievo non
facilmente ripetibile. IL DATO ANALITICO IN MICROBIOLOGIA E' DIVERSO DA QUELLO
FORNITO DALLA STRUMENTAZIONE AUTOMATICA. L'interpretazione è di chi legge.
Tante cellule non si trovano facilmente nel campione oculare come si trovano nel
campione endo cervicale. Nel tampone uretrale si parte da 10 cellule per campo
microscopico.L'idoneità del prelievo è data da queste cellule rotondeggianti
globose. Questa buona cellularità vuol dire che l'esame ha un alto valore
predittivo. Il tampone umido va fatto ruotare dopo aver fatto la reversione
palpebrale. VI SONO BATTERI ALL'INTERNO DELLE CELLULE NELL'INFEZIONE CRONICA.
Il medico del laboratorio è un medico clinico (clinos=letto) se va al letto del malato. Eversione della palpebra e scraping congiuntivale nel tarso superiore o nel fornice inferiore. Le infezioni da Candida sono post erpetiche. Si possono ottenere dei buoni vetrini per compressione o impressione e/o per scraping o grattamento. LA CITOLOGIA SI FA CON SCRAPING O IMPRESSIONE. La grave endoftalmite può essere da Pseudomonas aeruginosa o da Staph. aureus. La Chlamidia è un patogeno endo- cellulare obbligato. Con l'immunofluorescenza diretta studiamo una infezione che è andata avanti non è precoce nè cronicizzata.
Dal punto di vista delle correlazioni eziopatogenetiche si possono distinguere due differenti tipi di lesioni infettive dell’occhio. Le prime, che interessano il segmento anteriore, nella stragrande maggioranza riconoscono nella loro eziopatogenesi fenomeni che alterano l’ecosistema congiuntivale, sia per l’apporto di nuovi microrganismi a differente proprietà patogenetiche, sia per la differente localizzazione dell’ecosistema congiuntivale (valgano ad esempio le infezioni post-traumatiche o post-chirurgiche). Le seconde, interessano i tessuti ed i fluidi interni dell’occhio ed, in maggioranza, hanno eziologia molto diversificata e via di contagio ematogena. La nostra esperienza ci induce a ritenere che la diagnosi eziopatogenetica in laboratorio delle congiuntiviti e della patologia infettiva del segmento anteriore dell’occhio, da parte del microbiologo, debba essere basata sulla conoscenza di quelle proprietà biologiche dei microrganismi, grazie alle quali batteri e virus si organizzano sulla congiuntiva.
Prima di tutto va notato che la congiuntiva è uno dei tessuti dell’organismo colonizzati dai microbi, certamente sin dai primi momenti della vita extrauterina, e che questa colonizzazione avviene ad opera di una popolazione microbica molto poco definita. Nella Tabella 1 è elencato il microbiota facente parte dell’ecosistema oculare nelle varie epoche della vita e. per completezza, anche quello che si deposita sulla congiuntiva del cadavere, la cui conoscenza è basilare nei casi di trapianto della cornea. La componente microbica varia di poco, soprattutto in termini qualitativi, nel corso della vita, ma è interessante notare che tra i microrganismi residenti abituali sono indicati anche alcuni che hanno tutte le caratteristiche per essere ritenuti nettamente patogeni. È necessario, pertanto. un corretto approccio metodologico per definire l'ecosistema oculare, poter valutare come il microbiota residente, in via transitoria, possa essere modificato fino ad esprimere le proprie caratteristiche di virulenza ed indicare quali microrganismi alloctoni possano essere responsabili di una determinata infezione (1). Descriveremo, inizialmente i meccanismi che determinano la costituzione dell'ecosistema. indicando gli esempi tra i più attuali e più idonei dei meccanismi patogenetici delle congiuntiviti e, quindi, proporremo le metodologie diagnostiche più specifiche ed aggiornate che interessano le differenti patologie infettive dell'occhio.
Tabella 1 - MICROBIOTA CONGIUNTIVALE RESIDENTE
Neonato: Stafilococchi. Emofili, Neisserie. Corinebatteri.
Bambino: S.epidermidis, S.aureus, Str.viridans, B.catarrhalis.
Adulto: Str.viridans, S.epidermidis, S.aureus, Propionibacterium acnes, Emofili.
Cadavere: E.Coli, Ps.aeruginosa, Kl.pneumoniae, Flavobacterium.
L'ecositema congiuntivale è un sistema tendenzialmente equilibrato e biologicamente attivo, costituito da tutti i microrganismi che colonizzano l'habitat congiuntivale, e da quelle strutture e macromolecole, chimicamente e fisicamente definite, che rappresentano il locus anatomo-funzionale. Questo ecosistema si può ritenere bilanciato, se esistono interazioni equilibrate tra microrganismi ed habitat; per contro esso risulta disequilibrato se le interazioni sono favorevoli al microorganismo od all'ospite. Le componenti che possono, eventualmente, influenzare e perturbare questo equilibrio, rendendolo estremamente dinamico e molto labile, sono rappresentate da fattori tessutali, microbici ed ambientali. I primi sono dipendenti dalla struttura istologica del tessuto congiuntivale, dalle secrezioni facenti parte del film lacrimale, in particolare dalla produzione attiva a livello locale di immunoglobuline secretorie e dalla presenza di cellule antigenicamente competenti ed ad attività fagocitaria. Queste possono giocare un certo ruolo sia nella modulazione della colonizzazione come nella persistenza di alcuni microrganismi a livello congiuntivale. I fattori microbici sono quelli specifici di patogenicità, propri di alcune specie microbiche. Possiamo continuare a distinguere microrganismi residenti e commensali, siano essi transitori o permanenti, e microrganismi nettamente patogeni, ma risulterà chiaro che questa distinzione, come succede anche a livello dell’ecosistema lacrimale, lascia spesso indefiniti i termini del problema. Il terzo fattore della regolazione dell'ecosistema, che rende la patogenesi delle congiuntiviti più attuale e peculiare e che ha reso queste affezioni sempre più di difficile risoluzione terapeutica, è rappresentato dai fattori individuali ed ambientali:– gravi deficit del visus;– uso terapeutico non corretto delle protesi oculari;– inquinamento dell'aria e dell'acqua, da piombo, da gas di scarico, da prodotti industriali;– patologia ergoftalmica. Deriva da ciò la costituzione di un ecosistema. in una situazione estremamente dinamica, i cui fattori maggiormente variabili sono le modificazioni qualitative e quantitative dei microrganismi. I microrganismi tendono a permanere e ad aderire alla congiuntiva e, in generale, a stabilizzarsi e colonizzare su un tessuto attraverso un processo dinamico modulato dalla elevata o dalla modesta capacità adesinica, prescindendo dalle caratteristiche di virulenza. Il fenomeno dell'aderenza a cui consegue la moltiplicazione dei batteri, deve essere considerato quale momento iniziale della colonizzazione. Da esso ha origine formazione di quelle microcolonie che indicano il raggiungimento dell’optimum ambientale, da parte di quella specie batterica che riesce a moltiplicarsi, a colonizzare la superficie delle cellule ed a permanere stabilmente su quel tipo di tessuto. La comparsa delle microcolonie indica che i microrganismi sono riusciti ad organizzarsi. a creare un loro habitat particolare a stabilizzarsi, in via definitiva ed a rendere complesso il bio-film. In questa situazione dobbiamo pensare persistano e permangano i microrganismi a livello della superficie congiuntivale. La complessità e la dinamicità dell'ecosistema ulteriormente mantenuta dal fatto che le microcolonie esercitano un effetto "trapping" sui nutrienti assorbendo determinate sostanze, quali il ferro ionizzato, rendono ulteriormente ottimale la situazione metabolica dei microrganismi su quella superficie. Cominciano, successivamente, a comparire quei prodotti metabolici di digestione o di modificazione chimica di molecole semplici, quali polisaccaridi, ed altre macromolecole. Queste non fanno altro che complessare ulteriormente l’ecosistema. Si costituiscono situazioni molto definite e in tal modo si stabilisce anche una barriera protettiva, impermeabile a molte sostanze antibatteriche, ed anche i farmaci che noi siamo abituati ad utilizzare, seguendo le indicazioni ottenute dallo studio in vitro dell'antibiotico-sensibilità ma che, in vivo risultano essere inefficaci . Altro aspetto interessante di un ecosistema batterico è che questo tipo di complessazione del microbiota con le componenti secretorie, non si stabilizza soltanto sulle superfici cutanee e mucose, ma anche sui biomateriali, in particolare sui polimeri che vengono utilizzati per costruire le protesi. Sui biopolimeri, infatti, i batteri sono in condizione di aderire e di stabilizzarsi, di costituire microcolonie e biofilm completamente organizzati. Anche in questo caso viene ridotta od impedita l'azione dei macrofagi, perché essi non riescono ad arrivare a questo livello, ma agiscono solo sulle cosiddette forme planctoniche, cioè sui microrganismi ancora parzialmente liberi e non completamente aderenti. Allo stesso modo anche gli antibiotici e gli anticorpi poco riescono a modificare il biofilm e l'organizzazione macromolecolare complessa dell'ecosistema, una volta che questa si è stabilizzata .
Dal punto di vista patogenetico si evince che i microrganismi sono delle entità biologiche che hanno una elevatissima capacità di adattarsi fenotipicamente all' ambiente, grazie alle peculiari proprietà di modificare l'espressione genica delle loro caratteristiche di virulenza, in modo da adeguarsi alle diverse situazioni dell'ambiente in cui si trovano.
Si può tener conto, schematicamente, di due situazioni patogenetiche che corrispondono alle caratteristiche di virulenza di un microrganismo: il suo permanere sulla superficie e produrre macromolecole antigeniche, tossine o enzimi; oppure, come succede per microrganismi quali Chlamydiae e Virus, che si comportano da patogeni obbligati intracellulari, il penetrare con meccanismi attivi nella cellula ospite e replicarsi all' interno della cellula ospite. Il meccanismo di penetrazione intracellulare è seguito dal mascheramento antigenico e dalla inibizione della fusione fagosoma-lisosoma, è uno dei fenomeni che possono spiegare il permanere e il cronicizzarsi delle infezioni . Il microrganismo viene riconosciuto dai recettori specifici presenti sulla superficie della cellula e penetra in essa in quel fagosoma particolare, cioè in quella vescicola intracitoplasmatica all'interno della quale il microrganismo permane e si moltiplica, perché è in grado di impedire la formazione del fagolisosoma: in pratica, gli enzimi lisosomiali non arrivano mai nella vescicola in cui è presente il microrganismo e l'attività fagocitaria della cellula-ospite è fortemente ridotta. Si stabilisce. cosf, uno dei processi di cronicizzazione di una infezione, perché una volta che il microrganismo è rimasto dentro la cellula, e non necessariamente in una fase di latenza, può benissimo rimanerci anche in condizione di replicazione a basso livello. Se ne deduce che, una volta raggiunta questa situazione biologica, difficilmente potrà essere eradicato dal suo habitat. Da studi al microscopio elettronico si è potuto dimostrare come i corpi elementari di Chlamydia penetrino attraverso la superficie cellulare e come, di conseguenza. si determini la situazione di permanenza dei corpi elementari dentro i vacuoli citoplasmatici e la loro replicazione .
La comprensione dei meccanismi di produzione e di organizzazione macromolecolare dell'ecosistema oculare cosi come quella dei fattori ambientali e microbici, che svolgono un ruolo importante nella patogenicità delle infezioni del segmento anteriore dell'occhio, è basilare ai fini di un corretto approccio metodologico alla definizione eziologica delle congiuntiviti ed al loro trattamento terapeutico specifico, precoce e mirato.
Parimenti nella valutazione eziopatogenetica e nella corretta diagnosi di laboratorio di affezioni gravi quali, retiniti e panoftalmiti sono da tener presenti le condizioni immunitarie dell'ospite, che possono favorire particolari meccanismi di contagio e di penetrazione dei microrganismi e facilitarne la permanenza e la colonizzazione nei tessuti e nei fluidi interni dell'occhio.
EZIOLOGIA DELLE INFEZIONI OCULARI
L'eziologia e l'inquadramento nosografico delle differenti infezioni dell’occhio risultano di non facile definizione e classificazione, per la molteplicità dei microrganismi cui può essere dovuta questa particolare patologia e per la variabilità legata a condizioni fisiologiche (età ed attività lavorativa) o patologiche (immunodepressione, alterazioni metaboliche e vascolari croniche, deficit neurologici centrali e periferici) del paziente. Particolare importanza eziopatogenetica, in età neonatale, assumono Neisseria gonorrhoeae, Chlamydia trachomatis. Streptococchi di gruppo B, Candida albicans ed Herpesvirus, che possono contaminare la congiuntiva durante il parto per via naturale. Nei soggetti di età pediatrica l’eziopatogenesi delle congiuntiviti risulta molto più variabile, .ia per il possibile contagio da parte dei microrganismi già menzionati. ai quali si aggiungono Stafilococchi coagulasi positivi e negativi, Str.pyogenes, Haemophylus influenzae, Pseudomonas aeruginosa, Propionibacterium acnes, Adenovirus e Citomegalovirus, sia per alterazioni della reattività immunologica locale e generale. Nell’età adulta, fattori predisponenti l'azione patogena di tutti i microrganismi già indicati sono quelli ambientali e quelli legati all'attività lavorativa, agli sports ed agli hobbies, oltre che i deficit del visus. La patologia infettiva oculare da lesioni gravi e di difficile risoluzione terapeutica, quali infezioni post-traumatiche, postoperatorie, cheratiti, uveiti ed endoftalmiti, riconosce, infine, la più varia eziologia batterica, micotica e virale. La Tabella 2 riassume la patologia infettiva oculare, nella sua globalità, dal punto di vista eziologico.
Tabella 2 – PATOLOGIA INFETTIVA DELL'OCCHIO E SUOI ANNESSI.
| Lesione | Agenti eziologici | |||
| Cheratite suppurativa | Ps aeruginosa,Gram negativi, Miceti, Acanthameba | |||
| Cheratocongiuntivite virale | HSZ, HVZ, CMV,Adeno, Entero | |||
| Uveite anteriore (iridociclite) | infettiva | Virus parotite, Virus rosolia,HSV, HVZ,N. gonorrheae,Brucelle, Leptospira | ||
| non infettiva | ||||
| Uveite posteriore (corioretinite) | Toxoplasma gondii, M. tuberculosis,MOTT, Criptococcus neoformans, Toxocara canis, CMV | |||
| Endoftlamite | esogena | infezioni di ferite chirurgiche-traumatiche | ||
| endogena | setticemia | |||
| Congiuntivite | virale | Herpes Adeno | ||
| batterica | S. aureus, S. pyogenes, S. pneumoniae,H. influenzae,Gram negativi | |||
| da Chlamidia | C. trachomatis (sierotipi A-K) | |||
| dei neonati | N. gonorrhoeae, C. trachomatis, S. aureus | |||
| cronica | S. aureus, E. coli, Ps. aeruginosa, Moraxella lacunata, H.influenzae | |||
| allergica | microorganismi, farmaci, pollini, sostanze chimiche | |||
| Cellulite presettale | S. aureus, S. pyogenes,H. influenzae, Ps. aeruginosa, Anaerobi | |||
| Cellulite orbitale | acuta batterica | Aerobi/anaerobi.S. aureus | ||
| cronica | Micobatteri, Nocardia, Actinomiceti | |||
| Blefarite | acuta | Stafilococchi | ||
| cronica | Moraxella lacunata, Malassezia furfur | |||
| virale | Herpes, Mollusco contagioso | |||
METODOLOGIE DI LABORATORIO
Nelle infezioni dell'occhio e dei suoi annessi le richieste di diagnosi microbiologica possono essere routinarie, per affezioni a carico della congiuntiva e degli annessi palpebrali od urgenti ed indifferibili, in caso di lesioni che interessano i tessuti ed i fluidi interni .
Per il Microbiologo Clinico, quattro sono i momenti essenziali e qualificanti del procedimento diagnostico di laboratorio: (i) accertamento della idoneità e rappresentatività del prelievo; (ii) definizione di microbiota residente e microbiota patogeno; (iii) risoluzione di peculiari problematiche diagnostiche; (iv) valutazione ragionata dello spettro di chemiosensibilità.
4.1 Raccolta e trasporto del prelievo.
La prima fase dell'indagine microbiologica prevede la raccolta di un prelievo idoneo ed il suo corretto trasporto in laboratorio. Per ottenere un campione idoneo all’indagine microbiologica e rappresentativo della sede di infezione, è necessario che il prelievo venga eseguito il più precocemente possibile, in maniera asettica, precedentemente alla somministrazione locale o generale di farmaci ad attività antibatterica od antivirale, e nella fase più opportuna. in relazione ad eventuali interventi operatori. Risulta conveniente eseguire la raccolta del materiale da esaminare mediante tampone umido, nel caso di secrezioni e per l'isolamento dei batteri e dei miceti; mediante la spatola di Kimura nel caso di scraping congiuntivale. per l' identificazione e l'isolamento di Virus e Chlamydiae; mediante aspirazione se si tratta di esaminare raccolte di fluidi e/o secrezioni.
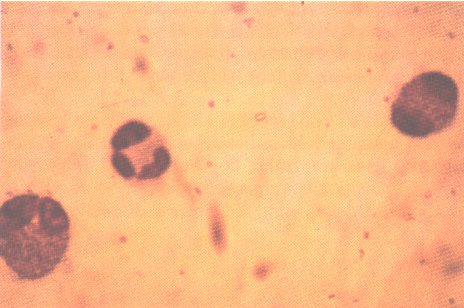
Fig 1-Eosinofilia in un prelievo di scraping congiuntivale colorato col metodo di Giemsa.
I tipi di prelievo che è opportuno eseguire non sono soltanto quelli necessari per le indagini identificative e colturali dei microrganismi patogeni ma anche il prelievo per l'esame della citologia congiuntivale e quello lacrimale e quello sierico per la valutazione della produzione di immunoglobuline specifiche (Tabella 3).
Tab. 3 – TIPI DI PRELIEVO
CITOLOGICO
LACRIMALE
SIEROLOGICO
IDENTIFICAZIONE DIRETTA (Scraping)
COLTURALE BATTERICO (Tampone)
4.2 Prelievo per citologia,
Il prelievo per l'esame citologico può essere molto utile per orientare la diagnosi eziologica della stragrande maggioranza delle infezioni congiuntivali. Esse forniscono un criterio valido per cercare l'agente eziologico, consentendo una preselezione dei terreni di coltura e delle metodologie di laboratorio da utilizzare del microorganismo patogeno e permette di fornire al Clinico una indicazione probante della diagnosi di sospetto
Il prelievo può essere osservato al microscopio dopo colorazione di Gram, che consente di studiare e valutare la componente batterica, la specie microbica prevalente, la presenza di forme ifali e/o miceliali. Mediante la colorazione di Giemsa si può attentamente individuare 1)la componente cellulare prevalente nel focolaio flogistico, 2) lo stato delle cellule epiteliali congiuntivali,3) la presenza di inclusioni citoplasmatiche: in particolare, le inclusioni da Chlamydia, la morfologia dei miceti. La colorazione con fluorescenza, mediante l'impiego di anticorpi monoclonali specifici, consente di diagnosticare direttamente la presenza di Chlamydiae, Herpesvirus ed Adenovirus.
In base alle considerazioni sulla composizione e sulla variabilità della popolazione microbica residente ed in relazione al quadro citologico osservato mediante le opportune colorazioni, è possibile avere un orientamento sufficientemente preciso sull'entità della lesione a livello dell'epitelio congiuntivale e corneale, sul tipo e sulla gravità della flogosi, sulla specie microbica prevalente (Tabella 4).
Il prelievo citologico consente, infine di mettere in evidenza, sia per quanto attiene alla diagnosi che alla prognosi, la presenza ed il numero dei linfociti B e T delle varie sottopopolazioni e fornisce in tal modo, la valutazione più completa della risposta immunitaria del soggetto a livello della sede di infezione.
Tab. 4 – CITOLOGIA DA SCRAPING CONGIUNTIVALE
| se troviamo queste cellule... | ...allora il significato diagnostico probabile è |
| PMN | Congiuntivite batterica, allergica, irritativa.Congiuntivite da adenovirus gigantopapillare |
| Linfociti, monociti | Congiuntivite da adenovirus, HSV, farmaci, cosmetici |
| Monociti | Chlamidia, HSV |
| Eosinofili | Congiuntivite allergica |
| Macrofagi, plasmacellule | Chlamidia |
| cellule cheratinizzate | Cheratite secca, AFL alterazione film lacrimale |
HSV=herpes simplex virus
4.3 Prelievo lacrimale.
Il prelievo lacrimale effettuato mediante capillare o per aspirazione, evitando la stimolazione farmacologica può esssere utilizzato: (i) per lo studio quantitativo e qualitativo della secrezione lacrimale, ad esempio nelle sindromi da secchezza lacrimale o nelle congiuntiviti a patogenesi allergica; (ii) per il dosaggio dell'attività antibatterico di componenti lacrimali quali il lisozima; (iii) per la valutazione, mediante metodiche basate sull’immunoperossidasi o su dosaggi nefelometrici del titolo anticorpale in SIgA specifiche sia nelle infezioni acute che in quelle croniche. Lo stesso tipo di prelievo può essere impiegato per la ricerca di antigeni specifici di virus, miceti o batteri con metodica immunoenzimatica, come in caso di uveiti, quando la carica batterica è minima.
4.4 Prelievo sierico.
Le indagini sierologiche possono trovare ampio campo di applicazione per valutare la reazione immunologica del paziente e per seguire l'evoluzione clinica dell'infezione.
Questo approccio può fornire un valido complemento alla diagnosi eziologica nel caso di infezioni congiuntivali o cheratitiche od endoftalmiche di cui possono essere agenti eziologici Adenovirus, Herpesvirus e Toxoplasma gondii. Più interessante sembra essere la valutazione prognostica, basata su prelievi sierici eseguiti ad intervalli di tempo tali da poter valutare le modificazioni del titolo anticorpale specifico. Nel caso di congiuntiviti da Chlamydia è possibile dosare non solo gli anticorpi sierici (IgG, IgM. IgA) ma anche le SIgA nel secreto lacrimale, lo studio completo del profilo immunologico del paziente può rappresentare una valida indicazione dell'evoluzione dell'infezione e dell'efficacia della terapia.
4.5 Scraping per identificazione diretta.
Lo scraping dalla sede dell'infezione per la raccolta di campioni biologici ad elevata cellularità è il prelievo migliore e più idoneo nei casi in cui si possa procedere all’identificazione diretta del microorganismo patogeno. Esso può essere eseguito con la spatolina di Kimura dalla cornea e da tutta la congiuntiva, oppure con un tampone di cotone alginato dai margini palpebrali e dalla punta del canale lacrimale. Nei casi di lesioni cherato-congiuntivali o di ulcere corneali, il materiale prelevato viene depositato solitamente su di un vetrino da microscopia, fissato ed opportunamente trattato per l’osservazione al microscopio (colorazione diretta, immunofluorescenza, DNA sonda biotinilata).
4.6 Campioni per indagini colturali batteriche.
I campioni per le indagini colturali devono esssere accuratamente insemenzati sui terreni appropriati per la ricerca dei differenti microrganismi. La definizione di microbiota di specie batterica patogena (cioè se quel batterio isolato è responsabile veramente della lesione n.d.r.) è da rapportare al grado di lesione infiammatoria, alle possibili concause di danno epiteliale e soprattutto alla carica batterica, che può risultare influenzata, ad esempio, dall'uso improprio di antibiotici.In alcuni tipi di infezioni oculari, può risultare buona nonostante il numero ridotto dei microrganismi presenti nel campione prelevato, procedere inizialmente all'arricchimento del prelievo in terreno adatto. Ad esempio nel caso di infezioni da anaerobi, in modo da aumentare la possibilità di individuare ed isolare i possibili agenti eziologici. In genere. la maggior parte delle specie eventualmente patogene può essere isolata con l'impiego di un ridotto numero di terreni selettivi accuratamente scelti. L identificazione definitiva dei microrganismi cresciuti sulle piastre di isolamento, può essere affidata all'esecuzione di test addizionali specifici, sia biochimici che sierologici, eseguiti con le apparecchiature automatizzate di uso comune nel laboratorio (tipo il Vitek n.d.r.). Il completamento delle indagini batteriologiche e micologiche richiede la valutazione della chemiosensibilità del microrganismo isolato. Uno schema molto sintetico del razionale che sta alla base delle metodologie identificative di laboratorio è riportato in Tabella 5.Molti dei microrganismi Gram positivi, isolati da campioni oculari sono repertabili anche tra il microbiota abitualmente residente nell'ecosistema oculare. La individuazione di essi quali agenti eziologici di determinate affezioni è da confrontarsi con il tipo di f1ogosi riscontrata, con le lesioni epiteliali diagnosticate clinicamente e con la definizione delle caratteristiche di patogenicità, con la carica microbica e con lo studio del profilo di chemiosensibilità (come detto piu' sopra n.d.r.). L'identificazione di microorganismi Gram negativi deve essere considerata significativa dal punto di vista eziopatogenetico, in particolare nel caso di ulcere corneali e di infezioni post-traumatiche e post-operatorie. Nei soggetti con deficit della reattività immunologica tutti i microrganismi possono comportarsi da patogeni opportunisti ed essere quindi responsabili di inazioni altamente invasive e rapidamente invalidanti.
Tab. 5 - SCHEMA DIAGNOSTICO DELLE CONGIUNTIVITI BATTERICHE

Molti dei microrganismi Gram positivi, isolati da campioni oculari, sono repertabili anche tra il microbiota abitualmente residente nell'ecosistema oculare. La individuazione di essi quali agenti eziologici di determinate affezioni è da confrontarsi con il tipo di flogosi riscontrata, con le lesioni epiteliali diagnosticate clinicamente, con la definizione delle caratteristiche di patogenicità, con la carica microbica e con lo studio del profilo di chemiosensibilità.
L’identificazione di microrganismi Gram negativi deve essere considerata significativa dal punto di vista eziopatogenetico, in particolare nel caso di ulcere corneali e di infezioni post-traumatiche e post-operatorie. Nei soggetti con deficit della reattività immunologica, tutti i microrganismi possono comportarsi da patogeni opportunisti ed essere quindi, responsabili di infezioni altamente invasive e rapidamente invalidanti.
Uno schema orientativo delle procedure da mettere in opera per identificare i microrganismi responsabili dei vari quadri di patologia oculare è riportato nella Tabella 6. Esso deve essere modulabile a seconda delle richieste del clinico, dei suggerimenti ottenuti con l'esame citologico. o delle condizioni cliniche del paziente. In ogni caso i prelievi devono essere effettuati dalla sede di lesione, raccogliendo con la giusta accortezza il materiale da esaminare ed evitando di aggravare e di estendere la lesione dei tessuti oculari. La colorazione con metodi standard o specifici per l'osservazione al microscopio del prelievo è mandataria, sia per orientare le procedure analitiche sia per fornire al clinico un primo riscontro eziologico, che può risultare basilare per il corretto trattamento terapeutico. Un sufficiente numero di terreni per la coltura e l'isolamento dei patogeni più frequenti e la dovuta attenzione nella ricerca dei microrganismi anaerobi contribuiscono alla corretta impostazione del lavoro del laboratorista.
Sebbene l'isolamento colturale e l'identificazione biochimica e/o antigenica dei batteri rappresentino il metodo di riferimento in laboratorio, l'ottimo grado di sensibilità e di specificità dimostrato dalla immunof1uorescenza diretta. con l'impiego di anticorpi monoclonali, la rende, in particolari casi una possibile alternativa diagnostica di più facile allestimento ed esecuzione. Una altrettanto valida metodologia identificativa, per la buona specificità e sensibilità in essa insita, è fornita dai test basati sulla utilizzazione di alcune attività enzimatiche caratteristiche dei vari microrganismi. In particolare. hanno assunto interesse crescente quali substrati specifici, per evidenziare attività enzimatiche proprie di Escherichia coli, Streptococcus homis, Enterococchi, Salmonella spp., Candida albicans, vari composti fluorofori che, idrolizzati dagli enzimi prodotti dai microrganismi sulla piastra di coltura, liberano 4-metilumbelliferone. Questo composto emette fluorescenza quando le piastre sono osservate con la lampada di Wood e permette l'identificazione delle colonie, con ampio margine di sicurezza.
4.7 Valutazione del profilo di chemiosensibilità.
Anche nel caso di infezioni dell'occhio e dei suoi annessi. il completamento dell'indagine batteriologica e micologica è raggiunto con lo studio del profilo di chemio-sensibilità dei differenti ceppi isolati nei confronti di quegli antibiotici od antimicotici che possono essere utilizzati per via generale, perché in grado di superare efficacemente la barriera emato-oculare. che per via topica-locale, sotto forma di pomate o colliri.
La diffusione di un antibiotico attraverso la barriera emato-oculare è influenzata da molteplici fattori: (i) il legame alle proteine plasmatiche ,solo la frazione libera del farmaco può diffonders; (ii) il grado di ionizzazione e la liposolubilità del farmaco; (iii) il peso molecolare, a parità di altre condizioni, quelli a più basso peso molecolare si distribuiscono più facilmente nei tessuti; (iv) lo stato di flogosi dei tessuti, dal momento che l' alterazione della permeabilità della barriera permette il passaggio di antibiotici non liposolubili.La penetrazione dei farmaci attraverso la cornea integra invece avviene per processi di trasporto legati alla particolare organizzazione anatomo-funzionale di questo tessuto: in particolare sostanze liposolubili penetrano sufficientemente bene, mentre quelle idrosolubili molto poco, per cui anche l'applicazione di questi antibiotici sotto forma di pomate o di colliri raramente riesce a fornire una concentrazione efficace del farmaco sulla cornea o nell'umore acqueo in assenza di lesioni corneali.
Nella situazione più frequente i risultati di una valutazione del profilo di chemiosensibilità di tipo qualitativo quale è possibile ottenere con il metodo di Bauer e Kirby, oppure con l'antimicogramma standardizzato, risulta di facile ed immediata utilizzazione da parte del medico curante. Bisogna tuttavia, notare che i risultati cosi ottenuti sono riferibili unicamente a concentrazioni sieriche dell'antibiotico che vengono raggiunte con una posologia media del farmaco somministrata ad un soggetto con buona funzionalità dei diversi organi ed apparati.
Nel caso delle infezioni congiuntivali, in effetti, i tassi di antibiotico, raggiunti in seguito ad una terapia per via generale, sono paragonabili a quelli raggiunti nel siero: il risultato di sensibilità o resistenza sarà quindi, di immediato ed efficace utilizzo (quindi il risultato di un antibiogramma in MIC è importante perchè confrontabile all'effettiva concentrazione dell'antibiotico in quel distretto n.d.r.)
Nei pazienti con infezioni in sedi dell'apparato oculare diverse dalla congiuntiva, difficilmente raggiungibili dall'antibiotico, il Microbiologo clinico dovrà utilizzare quelle metodologie analitiche in grado di esitare in un risultato quantitativo della chemio-sensibilità di quel dato batterio, valutando quindi la MIC o la concentrazione di break-point (la concentrazione di break point è in pratica la MIC 90 cioè la concentrazione di antibiotico che in vitro inibisce la crescita di almeno il 90% delle colonie o dei ceppi n.d.r.). In base a questi dati di laboratorio ed alle condizioni cliniche del paziente il Clinico potrà decidere quale farmaco e quale schema posologico utilizzare tenendo presente che solo la frazione non-ionizzata dell'antibiotico assorbito e ripartito nel circolo risulterà terapeuticamente efficace; la gran parte dell' antibiotico si legherà stabilmente alle proteine sieriche e non risulterà disponibile per l'azione antibatterica (6.7).
Nella Tabella 7 sono riportati gli antibiotici che vengono più frequentemente saggiati nei confronti dei batteri isolati da campioni oculari e gli antimicotici di più corretto impiego clinico (omissis)
In ogni caso l'antibioticoterapia delle infezioni oculari deve sempre tener presenti le interazioni tra batterio farmaco e paziente, che è indispensabile conoscere per una impostazione corretta e personalizzata della terapia. L'introduzione nella pratica clinica di un nuovo farmaco seppure suggerita dalla valutazione dei parametri in vitro, dovrebbe essere condizionata da e correlata ad un effettivo vantaggio terapeutico, od alla diminuzione degli effetti collaterali, oppure al miglioramento della compliance del paziente.
DIAGNOSTICA DI LABORATORIO
5.1 CELLULITE PRESETTALE
La cellulite presettale è una lesione infiammatoria del tessuto sottocutaneo delle palpebre, posto davanti al setto orbitale in un’area delimitata dall’attacco fibroso della cute ai bordi superiore ed inferiore dell’orbita. L’infezione, solitamente, consegue ad una ferita, ad un trauma ad una puntura e la sede di entrata del microrganismo infettante può essere inapparente al momento dello sviluppo della flogosi. L’elasticità della cute delle palpebre ed il distretto "relativamente chiuso" predispongono all’edema ed alla formazione dell’ascesso. I batteri più frequentemente causa dell’infezione sono: Staphylococcus aureus, Streptococcus gruppo A, che talvolta produce necrosi gangrenosa. Batteri anaerobi non sporigeni possono contribuire all’eziopatogenesi delle infezioni causate principalmente da batteri aerobi ed anaerobi facoltativi; tuttavia il loro ruolo come patogeni principali non è stato ancora del tutto definito. La mionecrosi del tessuto periorbitale, causata da Clostridi della gangrena gassosa, rappresenta una complicazione rara dei traumi periorbitali. Haemophilus influenzae può essere l’agente eziologico della cellulite presettale post-traumatica in soggetti di ogni età, ma più frequentemente produce edema non suppurativo delle palpebre e della congiuntiva tarsale nei bambini dai 6 mesi ai 3 anni di età. Pseudomonas aeruginosa ed altri patogeni gram negativi rappresentano agenti eziologici di infezioni presettali nei soggetti immunocompromessi.
In assenza di una lesione aperta o di un drenaggio, l'aspirazione del materiale purulento dalla sede di infezione, dovrebbe poter consentire l'isolamento del microrganismo patogeno senza contaminazione da parte del microbiota presente sulla cute. Nella lesione suppurativa presettale, che interessa principalmente la palpebra superiore, l'incisione per la raccolta del campione da esaminare va fatta sotto la rima fronto-orbitale, all'altezza del terzo laterale della palpebra; in quella che interessa principalmente la palpebra inferiore nel punto di massima tensione, ben al di sotto della rima orbitale; in ogni caso bisogna rendere minimi i possibili danni alle altre strutture oculari. Il materiale raccolto, mediante una siringa sterile, va inoculato direttamente nei terreni di coltura preselezionati per aerobi od anaerobi ed utilizzato per eseguire un preparato da osservare al microscopio dopo colorazione col metodo di Gram.
5.2 ERISIPELA OCULARE
Consiste in una rara forma di cellulite acuta causata da Streptoccus di gruppo A. L'infezione è inizialmente caratterizzata da eruzioni maculari ben delimitate che tendono ad allargarsi e la cute a divenire rosso-cremisi calda ed indurita. Anche in questo caso non è solitamente visibile la ferita o la lesione iniziale dell'infezione. Diversamante dalla cellulite presettale post-traumatica, l'infiammazione può interessare anche lo spazio periorbitale, causando proptosi, edema congiuntivale e gravi limitazioni della mobilità oculare. Per mettere in evidenza lo Streptococco di gruppo A è preferibile effettuare il prelievo strofinando un tampone di cotone alginato imbevuto di brodo sulla congiuntiva tarsale e sul fornice di entrambi gli occhi ed inoculando il prelievo su agar-sangue. L’isolamento colturale del microrganismo e l'aumento del titolo anti-streptolisinico nel corso della convalescenza possono confermare la diagnosi di laboratorio e dare indicazioni prognostiche.
5.3 CELLULITE ORBITALE
È un'infezione molto grave che può portare alla cecità, alla trombosi settica del seno cavernoso e ad infezioni intracraniche. La via di ingresso principale dell'infezione è rappresentata da traumi o da interventi chirurgici sull'orbita o dal propagarsi di panoftalmiti e di infezioni dei seni paranasali. La diagnostica eziologica può essere molto complessa.
Cellulite Orbitale Acuta Batterica. L'agente eziologico è determinato dalla via di infezione: nei casi di insorgenza in seguito a trauma è principalmente S.aureus, ma si possono verificare anche infezioni miste o da microorganismi anaerobi; nei casi associati a panoftalmite i patogeni più comuni sono S.aureus. St.pneumoniae, Ps.aeruginosa, ma molti altri batteri possono rappresentare l'agente eziologico; nei casi associati ad infezioni dei seni paranasali si repertano frequentemente S.aureus. Streptococcus di gruppo A. St.pneumoniae. H.influenzae nei bambini di età inferiore ai 5 anni, batteri Gram negativi nei soggetti immunodepressi e microrganismi anaerobi non sporigeni. Questa infezione dei tessuti dell'orbita è caratterizzata da febbre. leucocitosi, edema palpebrale, proptosi ed iperemia congiuntivale con limitazione della motilità oculare. Il prelievo effettuato in modo appropriato, per aspirazione, deve essere inoculato rapidamente negli adatti terreni ed utilizzato per allestire un preparato per l'osservazione microscopica.
Mucormicosi. È un'infezione micotica potenzialmente letale dei seni paranasali (non mettere le dita nel naso! -:)) e dell'orbita causata da miceti dell' ordine dei Mucorales. Il microrganismo colonizza a livello dei turbinati e dei seni nasali. penetra nella tunica muscolare dei vasi arteriosi e raggiunge per via vascolare e per diffusione diretta i tessuti dell'orbita. L'infezione è più frequente nei pazienti che soffrono di diabete mellito, sia in forma lieve che scompensata, nei soggetti sottoposti a terapie immunosoppressive o con farmaci citostatici, nei cirrotici ed in quelli affetti da malattie reticoloendoteliali. Lesioni orbitali in soggetti con malattie croniche gravi e debilitanti devono suggerire l'eziologia da Mucorales ed implicano obbligatoriamente la conferma diagnostica in laboratorio vista la gravità dell'infezione e la necessità di una terapia rapida e specifica. Il prelievo bioptico dalla sede di necrosi tissutale e l' osservazione al microscopio, dopo colorazione con ematossilina-eosina possono essere sufficienti per porre diagnosi eziologica.
Cellulite orbitale cronica. È un'infezione progressiva dei tessuti orbitali che può insorgere subdolamente dopo interventi chirurgici sulla retina o sulla cavità orbitale e riconosce quali agenti eziologici, i microrganismi patogeni comuni alle altre forme di cellulite orbitale ed inoltre Mycobacteriurn, Nocardia, Actinomyces e miceti filamentosi. Il prelievo, costituito dal materiale di drenaggio deve essere inoculato su agar-sangue, Lowenstein-Jensen. Sabouraud e brodo BHI ed utilizzato per allestire le colorazioni specifiche per batteri. micobatteri e miceti.
5.4 INFEZIONI DEL CANALE E DELLE GHIANDOLE LACRIMALI
S.aureus. Sr.pneumoniae, Streptococcus di gruppo A sono gli agenti eziologici della Dacrioadenite che è l' infezione acuta delle ghiandole lacrimali. Il contagio è causato dal microbiota che colonizza la congiuntiva e che, attraverso i piccoli dotti lacrimali del fornice sopratemporale o per via ematogena raggiunge la ghiandola. Lo stato di flogosi è molto evidente ed è accompagnato da secrezione congiuntivale mucopurulenta e talvolta da suppurazione. Il prelievo va effettuato con tampone di calcio alginato, da entrambe le mucose congiuntivali, e dai fornici ed inoculato in agar sangue ed agar cioccolato ed utilizzato per allestire preparati per l'osservazione microscopica. È, preferibile far precedere la raccolta dall'instillazione di poche gocce di anestetico. Le forme ematogene di dacrioadenite possono essere complicanze della gonorrea, e di infezioni virali quali parotite, mononucleosi, inf1uenza: le forme croniche possono presentarsi in seguito a congiuntivite da Chlamydia trachomatis e le forme croniche granulomatose possono essere causate da Treponema pallidum, Mycobacterium tuberculosis, Mycobacterium leprae, MOTT, Nocardia, e da miceti filamentosi. Per porre la diagnosi di laboratorio, in questi ultimi casi, è necessario eseguire la biopsia della ghiandola lacrimale che verrà sia analizzata dal punto di vista istologico che utilizzata per l'inoculo su terreni selettivi e per l'osservazione al microscopio a luce diretta ed in campo oscuro.
La Canalicolite è una rara infezione della punta e del canale lacrimale che si presenta con un'evidente flogosi della punta del canale e secrezione di essudato purulento dal canale, con andamento, talvolta rapidamente evolutivo. L' agente eziologico nella maggior parte dei casi è rappresentato da Actinomyces israelii e da Arachnia propionica; spesso l'infezione è sostenuta da un microbiota misto, costituito da aerobi ed anaerobi, con notevole difficoltà nell'interpretazione diagnostica, dovuta anche alla probabile contaminazione congiuntivale. La semplice compressione del canale lacrimale facilita la raccolta del campione da esaminare. che va inoculato sugli opportuni terreni di coltura. Il trattamento terapeutico, mirato e corretto, deve tendere alla detersione completa del focolaio flogistico.
La Dacriocistite può rappresentare una evoluzione delle affezioni precedenti: essa si verifica quando sono presenti condizioni che impediscono il deflusso del canale lacrimale. In questi casi la raccolta del campione può essere effettuata mediante aspirazione transcanalicolare e comunque risulta utile effettuare la coltura del prelievo dalla mucosa congiuntivale. La diagnosi microbiologica non è mai semplice e richiede l’utilizzazione di un ampio numero di terreni per l'isolamento di tutti i possibili patogeni.
5.5 BLEFARITE
Blefarite batterica. È l'infezione dei margini palpebrali causata, quasi esclusivamente. da Stafilococchi coagulasi-positivi e coagulasi-negativi. Si presenta come una infiammazione acuta, fino all ulcerazione, del margine palpebrale associata a cellulite della palpebra e può verificarsi, comunemente, in seguito ad un'infezione da virus erpetici. Talvolta gli agenti eziologici sono rappresentati da batteri gram negativi. La lesione può tendere a cronicizzare con la formazione di crosticine e l'ispessimento del margine palpebrale, ordeola, perdita delle ciglia edema congiuntivale e lesioni conseguenti sull' epitelio corneale. Queste lesioni sono presenti anche nella blefarite angolare in cui è interessato anche il canto laterale e che è causata da Moraxella lacunata. Il prelievo in ogni caso va effettuato mediante tampone alginato imbevuto di brodo di coltura e strofinato sul margine palpebrale; il tampone di ciascun occhio viene inoculato su agar sangue e sugli altri terreni ritenuti necessari.
Blefarite virale. Herpes simplex ed Herpes zoster sono agenti eziologici della blefarite virale, che si presenta con eruzione vescicolare delle palpebre e degli annessi oculari. La distinzione tra la blefarodermite da HSV ed HZV ha importanti implicazioni per la terapia. Il prelievo ottimale in questi casi è rappresentato dallo scraping della zona interessata; i procedimenti diagnostici consigliabili sono quelli che consentono l'identificazione rapida e specifica del virus ad esempio l'immunofluorescenza diretta (vedi congiuntivite virale).
5.6 CONGIUNTIVITE
Le congiuntiviti sono le più frequenti infezioni dell' occhio nonostante la protezione fornita dal movimento palpebrale, dall'azione antibatterica delle lacrime, dalla continuità e dalla struttura dell'epitelio congiuntivale, dall'effetto equilibrante del microbiota residente. Le infezioni congiuntivali hanno eziopatogenesi differente a seconda della via di contagio, ed incidenza variabile a seconda dell’età, della funzionalità visiva, dell'attività giornaliera prevalente e delle condizioni immunitarie del soggetto. Il contagio comunemente avviene da parte di fomites trasportati dall’aria, nello stesso soggetto per via mani-occhi, per diffusione dell'infezione dagli annessi oculari e, raramente, per via ematogena. L'eziologia può variare da quella batterica, a quella micotica a quella virale ed, in ogni caso, impone una diagnosi eziologica basata sulle più moderne, specifiche e sensibili metodologie.
Congiuntivite batterica.
Si presenta come una infezione acuta, per insorgenza e decorso, caratterizzata da edema bilaterale, iperemia e secrezione congiuntivale e talvolta, linfoadenopatia regionale (Figura 4 di pag. 42). I principali agenti eziologici di questo tipo di infezione sono: S.aureus, Streptoccus di gruppo A, St.pneumoniae, H.influenzae, Neisseria gonorrhoeae. Nei bambini al di sotto dei tre anni di età deve essere considerato tra gli agenti eziologici di congiuntivite batterica, soprattutto H.influenzae, mentre N.gonorrhoeae deve essere ricercato in ogni paziente che presenti una congiuntivite rapida, progressiva, purulenta. Tra i microrganismi meno frequentemente implicati quali agenti eziologici di congiuntivite, vanno considerati Enterobacteriaceae e Pseudomonas aeruginosa, che sono in grado di provocare gravi forme di congiuntivite nei soggetti immunocompromessi, negli ospedalizzati per lungo tempo ed in quelli sottoposti ad interventi chirurgici sull'occhio.
Il prelievo dall'epitelio congiuntivale, sede della flogosi, deve essere in tutti questi casi ottenuto. senza procedere all' instillazione di anestetici locali, strofinando delicatamente un tampone alginato sulla superficie tarsale e sul fornice congiuntivale: il materiale raccolto, nel più breve tempo possibile, deve essere inoculato sui terreni adatti all'isolamento. Anche il prelievo, ottenuto per scraping delicato della congiuntiva, risulta molto utile per l'identificazione microscopica del microrganismo causa dell'infezione: cosi' come la valutazione delle componenti cellulari del secreto congiuntivale possono orientare validamente verso la diagnosi eziologica. consentendo di distinguere tra forme infettive, allergiche ed irritative. La congiuntivite batterica acuta è caratterizzata, ad esempio, dalla presenza in numero notevole di granulociti polimorfonucleati, quella allergica dalla predominanza di eosinofili.
Congiuntivite dei Neonati.
Rappresenta una particolare entità nosologica che riconosce tre differenti modalità di contagio ed un'eziologia peculiare. La congiuntiva del neonato può essere infettata per via ascendente a partire dalla vagina o dalla cervice dell'utero materno, in seguito a rottura prematura delle membrane (parto prematuro ndr); per contaminazione da secrezioni infette dall'apparato genito-urinario materno al momento del parto, per contaminazione da parte di oggetti infetti o di persone infette durante il periodo neonatale. Gli agenti eziologici possono essere sia batteri (S.aureus, Sr.pyogenes, N.gonorrhoeae. C.trachomatis, Ps.aeruginosa) che virus (HSV, HZV). La diagnosi eziologica si impone in relazione ai gravi danni che possono conseguire ad un trattamento terapeutico inadeguato.
Congiuntivite da Chlamydia.
L'approccio metodologico più corretto da utilizzare per la diagnosi di questo tipo di infezioni. non può prescindere dalle conoscenze delle proprietà biologiche e patogenetiche di questi microrganismi (8). Le manifestazioni cliniche delle congiuntiviti da Chlamydia sono rappresentate dalle forme acute e dalle forme croniche, sia nel neonato che nel bambino, e nell' adulto. I sierotipi di C.trachomatis responsabili di infezioni oculari sono tutti quelli classificati con le lettere da A a K. Nel neonato il contagio avviene soprattutto durante il passaggio nel canale del parto o per rottura precoce delle membrane oppure per contagio dall'ambiente: nel bambino e, soprattutto nel giovane adulto, per contatto inter-umano e riconosce alcune concause quali quelle da inquinamento ambientale, da acque delle piscine e le protesi oculari (lenti a contatto).
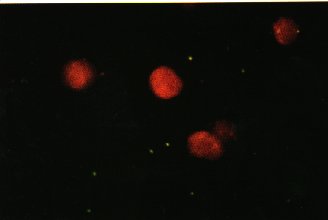
Fig 2-Colorazione in IF diretta di uno scraping congiuntivale.Sono evidenti numerosi corpi elementari di Chlamidia tracomatis x400
I prelievi, ad elevata cellularità esfoliativa, vengono eseguiti per scraping congiuntivale. L’isolamento del microrganismo, effettuato mediante la coltura del prelievo, con procedura standardizzata. su cellule McCoy trattate con cicloeximide, rappresenta il metodo standard di riferimento (ma chi lo fa in Italia? ndr). L’identificazione diretta si può eseguire mediante Immunofluorescenza diretta. Nella Figura 5 di pag. 42 è presentato un campione da scraping congiuntivale positivo per Chlamydia all’immunofluorescenza diretta, eseguita utilizzando un anticorpo monoclonale anti-LPS fluoresceinato.
Nel nostro laboratorio l’identificazione sul prelievo congiuntivale viene effettuata, oltre che con una metodologia ampiamente diffusa, quale l'immunofluorescenza diretta, anche mediante un approccio diagnostico attuale quale quello rappresentato dall’ibridizzazione in situ, mediante DNA probe marcato con nucleotidi biotinilati (oggi si vanno diffondendo i metodi con le sonde di DNA in automazione come nell'LCX Abbot ndr )(9).
Questa metodica permette di mettere in evidenza quantità minime di DNA del microrganismo presente all'interno delle cellule del paziente. La reazione si basa sull'alta omologia di sequenza tra il DNA del campione ed il DNA probe marcato con biotina. La reazione avviene in tre fasi: la prima è una fase di ibridizzazione, che si verifica per effetto della temperatura, tra il DNA del microrganismo. eventualmente presente all'interno delle cellule del preparato ed il DNA-probe, che viene aggiunto al campione da esaminare. Nella seconda fase della reazione il DNA-sonda marcato con biotina viene fatto reagire con il complesso rivelatore costituito dalla miscela streptoavidina-enzima: l'alta affinità della streptoavidina per la biotina fa si che si formi un legame specifico. Nella terza fase l'aggiunta di un substrato specifico per l'enzima legato alla streptoavidina consentirà di rilevare il DNA del microrganismo (10).
Il probe attualmente più usato nei kits commerciali è quello costituito dal plasmide criptico di 7 kbp, presente in tutti i sierotipi di Chlamydia trachomatis finora studiati ( 1 1 ). Nella Figura 6 di pag. 43 è presentato un campione da scraping congiuntivale, insemenzato su monostrato di cellule McCoy. positivo per Chlamydia trachomatis all'ibridizzazione mediante DNA probe e nella Figura 7 di pag. 43 un campione congiuntivale positivo all' ibridizzazione diretta in situ.
La diagnosi delle infezioni congiuntivali da Chlamydia può essere completata dal dosaggio, mediante una metodica in immunoperossidasi su campioni lacrimali delle SIgA e sierici delle IgA e delle IgG. Il campione, opportunamente diluito, viene depositato su dei vetrini preparati contenenti cellule infettate con Chlamydia che esprimono antigeni clamidiali. Dopo questa prima fase di reazione. si aggiunge un anticorpo anti IgG o anti IgA, marcato con la perossidasi: la terza fase della reazione prevede l'aggiunta del substrato specifico: lo sviluppo della colorazione perinucleare nell’interno delle cellule, indica l'avvenuta reazione tra l'anticorpo presente nelle lacrime o nel siero e l'antigene clamidiale presente sulle cellule. Questo test assume notevole importanza, sia in termini diagnostici se eseguito nella fase acuta dell'infezione, dimostra titoli anticorpali elevati sia in termini prognostici, perché il titolo delle SIgA sembra correlabile con la guarigione clinica dell'infezione (12). Nella Figura 8 (a-b) di pag. 43 sono mostrati. rispettivamente un campione di lacrime risultato negativo ed uno positivo all'immunoperossidasi per la presenza di IgA anti-Chlamydia.
Congiuntivite virale.
Un notevole incremento di specificità e di sensibilità. oltre che di rapidità, si è raggiunto recentemente nella diagnosi eziologica delle congiuntiviti da virus. (13). Anche in questi casi una corretta diagnosi eziologica presuppone l'effettuazione di prelievi congiuntivali ottenuti mediante scraping sulle zone di flogosi o scraping corneale. Il trasporto del campione viene effettuato in provetta contenente terreno idoneo. Le metodologie diagnostiche prevedono l'isolamento su cellule permissive, quale metodiche standard di riferimento e l'identificazione diretta mediante immunofluorescenza diretta. Oppure come di uso sempre più comune, mediante ibridizzazione in situ col DNA-probe. Inoltre, è sempre buona norma eseguire il dosaggio sierologico, per valutare il titolo anticorpale specifico contro gli antigeni virali. Come abbiamo già detto, i virus maggiormente responsabili delle infezioni del segmento anteriore dell'occhio, sotto forma di cherato-congiuntiviti, sia in età pediatrica che nell'adulto, che nel soggetto immunocompromesso sono Adenovirus, HSV, HZV e Citomegalovirus. Pur riconoscendo la piena validità ai vari approcci metodologici per la diagnosi di infezioni virali del segmento anteriore dell'occhio, noi preferiamo procedere all'identificazione diretta di questi virus mediante ibridizzazione in situ con DNA probe, perché più sensibile e specifica. La positività a questo tipo di indagine è difatti, correlabile alla replicazione virale nelle cellule infettate ed è, quindi, segno probante di infezione attiva. Nella Figura 9 di pag. 44 è riprodotto un preparato al microscopio di campione da scraping congiuntivale positivo per Herpes all'ibridizzazione in situ; nella Figura 10 di pag. 44 un campione positivo per Adenovirus.
5.7 CONGIUNTIVITI ALLERGICHE
La patogenesi e la diagnostica delle congiuntiviti allergiche, di recente, sono state definite in modo più dettagliato grazie alle nuove conoscenze acquisite nel campo dell'allergologia. Col termine congiuntivite allergica, comunemente si definiscono quelle flogosi congiuntivali nelle quali il meccanismo patogenetico preponderante è quello mediato dalle IgE, tipico dell'allergia di tipo I e nelle quali i sintomi clinici, provocati dal rilascio dei mediatori chimici, interessano non soltanto la congiuntiva ma anche la mucosa nasale (rinocongiuntivite). Altre sindromi allergiche congiuntivali sono rappresentate dalla cheratocongiuntivite atopica, che si presenta nei soggetti sofferenti di dermatite atopica; dalla congiuntivite primaverile, con andamento stagionale: dalla congiuntivite giganto-papillare, frequente nei portatori di lenti a contatto; dall'allergia congiuntivale da contatto, che rappresenta il coinvolgimento oculare dell'eczema cutaneo da contatto (Figura 11 di pag. 44). Le reazioni allergiche a livello della congiuntiva ma anche della mucosa nasale e, talvolta, della cornea sono fenomeni che interessano fino al 15-20% della popolazione e, quindi, richiedono una grande attenzione nel loro inquadramento diagnostico. Un approccio corretto a questa problematica comprende: i) esame della citologia congiuntivale e del citocentrifugato lacrimale: ii) dosaggio delle IgE lacrimali totali e specifiche nella fase acuta ed in quella di remissione della malattia; iii) valutazione dell'istamina lacrimale nelle diverse fasi della malattia; iv) test di provocazione congiuntivale specifica.
La rinocongiuntivite allergica è clinicamente molto ben evidente per i segni di arrossamento congiuntivale, lacrimazione e fotofobia, associati a quelli nasali. La diagnosi, che è facilitata da una attenta anamnesi personale e familiare del paziente. può essere precisata dalle prove allergologiche, dallo studio delle popolazioni linfocitarie congiuntivali e dal test di stimolazione congiuntivale.
La cheratocongiuntivite atopica è la manifestazione oculare dei soggetti atopici; presenta un andamento cronico con remissioni e riacutizzazioe e può esitare in complicanze quali cataratta e cheratocono.
La congiuntivite primaverile è una flogosi ipertrofica, papillare, bilaterale della congiuntiva superiore. che si presenta. più frequentemente in età prepuberale, in pazienti con una anamnesi familiare e personale di manifestazioni atopiche, quali ad esempio l'asma bronchiale. In questi soggetti si possono mettere in evidenza elevate concentrazioni lacrimali e sieriche di IgE e la presenza a livello congiuntivale, di infiltrati cellulari costituiti da linfociti, plasmacellule, basofili, eosinofili e mastociti: particolare rilievo è assegnato alla presenza di linlociti T capaci di sintetizzare IL-4 ed amplificare la risposta allergica, innescata dalla presentazione degli allergeni alle cellule T2.
L'allergia oculare da contatto è legata alla particolare sensibilizzazione nei confronti di sostanze contenute nei colliri, nei liquidi detergenti delle lenti a contatto e nei cosmetici; la diagnosi è basata sul test da contatto "patch test".
In ogni caso il test di provocazione congiuntivale (TPC) e la valutazione della funzionalità delle cellule linfocitarie congiuntivali rappresentano, dopo le prove allergometriche, ed il dosaggio delle IgE le indagini diagnostiche che consentono di risolvere la problematica eziopatogenetica delle forme allergiche congiuntivali e, quindi, di impostare correttamente il trattamento terapeutico. Nel test di provocazione congiuntivale, la stimolazione viene eseguita instillando nel sacco congiuntivale del paziente, che ha opportunamente interrotto per tempo l’assunzione di farmaci antiallergici, una goccia, ogni 15 minuti. della soluzione contenente il possibile allergene, precedentemente individuato con i test cutanei, in diluizioni decrescenti a partire da 1:10.000. L'instillazione si effettua in uno dei due occhi e si utilizza l'occhio controlaterale come controllo negativo. La positività al test è dimostrata dalla comparsa dei sintomi propri dell'allergia nell'occhio trattato (Figura 12 di pag. 45).
La valutazione della funzionalità delle cellule linfocitarie congiuntivali deve essere raffrontata con la loro distribuzione nel tessuto congiuntivale del soggetto normale, che è diversa a seconda dello strato istologico preso in esame (epitelio, stroma, follicolo): nell'epitelio sono presenti solo linfociti T, la maggioranza dei quali del tipo suppressor con un rapporto CD4/CD8 di 1:2; nella sostanza propria i linfociti T CD4 e CD8 sono ugualmente rappresentati: nella zona follicolare prevalgono i linfociti B. Gli infiltrati linfocitari possono essere caratterizzati funzionalmente su sezioni istologiche colorate con immunofluorescenza o con immunoperossidasi. Più recentemente è stato possibile standardizzare metodologie per lo studio delle popolazioni linfocitarie, mediante immunofluorescenza con anticorpi monoclonali specifici nei confronti dei marcatori di membrana. In questo caso il prelievo viene ottenuto per centrifugazione dell'aspirato congiuntivale. Con questa metodica sono stati confermati sia i dati ottenuti sulla congiuntiva del soggetto normale sia quelli ottenuti sulla congiuntiva dei soggetti allergici che mostrano in questi ultimi un rapporto invertito a favore dei CD4 od una uguale presenza di entrambi i tipi di linfociti T. In conclusione, nella patogenesi delle varie forme di congiuntiviti allergiche giocano un ruolo determinante sia meccanismi allergici di tipo I, che presuppongono l'interazione delle IgE, leganti gli allergeni, con i recettori presenti sui basofili ed i macrofagi, sia di tipo IV, che presuppongono l'interazione tra linfociti T (14).
5.8 CHERATITE
Fattori esogeni e modificazioni dello habit corneale, quali quelle da alterazione del film lacrimale. possono agire da concause nella patogenesi delle differenti infezioni corneali sostenute da batteri, virus e miceti. Questi agenti eziologici sono accomunati non tanto dalle loro precipue caratteristiche di patogenicità, ma dal fatto di essere capaci di invadere il tessuto corneale, specie in presenza di microlesioni. La sintomatologia. così come le lesioni più evidenti solitamente si presentano a carico di un solo occhio. Le infezioni corneali, qualunque sia la loro eziopatogenesi, risultano lesioni molto gravi, invalidanti e richiedono una conferma diagnostica rapida e precisa.
Cheratite batterica
La principale via di contagio, nel caso della cheratite batterica, è quella costituita dalle lesioni di continuo dell'epitelio corneale, provocate da microtraumi o da corpi estranei. In questi casi molti sono i microorgansimi che possono colonizzare e provocare reazioni flogistiche. mentre nel caso di epitelio corneale integro N. gonorrheae N.meningitidis, C.difteriae sono i soli microorganismi in grado di invadere il tessuto e svolgere la loro azione patogena. La cheratite batterica è caratterizzata da dolore acuto, ulcerazione dell’epitelio e, talvolta, dello stroma corneale, secrezione congiuntivale. Oltre a quelli indicati in precedenza, S.aureus, St.pneumoniae, Ps.aeruginosa, Citrobacter, Klebsiella, Enterobacter, Serratia, Proteus sono gli agenti eziologici di questo tipo di lesione oculare. Mycobacterium chelonei, e Mycobacterium fortuitum, meno frequentemente, provocano lesioni ulcerative corneali croniche.
Cheratite micotica
La cheratite micotica è causata. in prevalenza, da miceti saprofiti, filamentosi (Fusarium solani, Aspergillus, Acremonium, Curvularia) e da lieviti (Candida albicans) che colonizzano su lesioni dell’epitelio corneale, provocate da traumi o da precedenti infezioni. oppure sull'epitelio corneale integro di pazienti immunodepressi (Figura 13 di pag. 45).
È buona norma, per una precisa diagnosi eziologica delle cheratiti infettive in laboratorio, sia procedere al prelievo dalla congiuntiva ed alla coltura dei microrganismi sia eseguire contemporaneamente il prelievo, con la spatola di Kimura, mediante scraping delle varie zone ulcerate o suppurate presenti sulla cornea.
È necessario allestire vetrini per le colorazioni di Giemsa, di Gram e per colorazioni speciali. Il prelievo dovrebbe essere inoculato, in successione, su agar-sangue, agar cioccolato, agar Sabouraud, brodo tioglicollato, agar anaerobi. Brain heart infusion. È estremamente importante ottenere campioni multipli per ciascun terreno, preparare vetrini da tutte le aree di suppurazione, poiché la localizzazione di microrganismi replicantisi può variare in funzione di molti fattori. Tutta la procedura richiede circa 15-20 punti di scraping. che possono essere ridotti notevolmente se il tipo di lesione non appare particolarmente grave e non c'è pericolo di perforazione.
L'opacamento del fluido della camera anteriore (ipopion), che spesso accompagna la cheratiie microbica,. non contiene batteri, ma soltanto cellule infiammatorie: il suo prelievo per aspirazione è, pertanto, controindicato, tranne che nelle suppurazioni dello stroma corneale profondo, che non possono essere sottoposte a prelievo standard e che suggeriscono l'invasione della camera anteriore da parte dei microrganismi responsabili dell'infezione. Campioni del fluido dovrebbero essere inoculati sugli stessi terreni ed osservati al microscopio secondo le procedure usate per i prelievi ottenuti in corso di endoftalmiti. Dal momento che i batteri Gram negativi sono responsabili del 60% delle cheratiti batteriche,un test rapido ed efficace per la definizione diagnostica è quello basato sul Limulus, per il dosaggio dell' attività endotossica del lipopolisaccaride.
Cheratite da Acanthamoeba
È questa una particolare ameba presente nell'ambiente, che può comportarsi da agente eziologico di una rara forma di cheratite cronica. La lesione è caratterizzata dalla suppurazione multifocale, ad anello. dello stroma corneale in soggetti che hanno ricevuto terapia locale con corticosteroidi o che presentavano ulcerazioni pregresse. Il prelievo viene eseguito con le modalità precedentemente indicate. Il campione viene utilizzato per allestire preparati per le colorazioni di Gram e di Giemsa. che consentono di evidenziare le cisti e per eseguire l'inoculo su agar sangue oppure su agar base cui viene depositato uno strato di cellule di Escherichia Coli inattivate al calore (di cui l'ameba si nutre ndr).
Cheratite virale
Le infezioni congiuntivali virali, causate da HSV, HZV ed Adenovirus sono prevalentemente delle cheratocongiuntiviti con lesioni più o meno gravi a livello della cornea. Il virus Herpes simplex causa ricorrenti cheratiti, anche senza lesioni congiuntivali apparenti, oppure cheratocongiuntiviti complesse, soprattutto in pazienti con deficit immunologici ad eziologia differente. L'esame con la lampada a fessura mostra al Clinico la cheratite erpetica con il caratterisetico aspetto "dendritico", provocato dalle lesioni puntuate e lineari oppure una lesione ulcerativa di forma irregolare "a carta geografica" (Figure 14, 15 di pag. 45).
In tutti questi casi, non è facile ed agevole effettuare prelievi dalla ulcerazione corneale o dall'epitelio sede della flogosi, anche per il possibile rischio di lesionare il tessuto: è preferibile, quindi, raccogliere materiale mediante l’esecuzione di un tampone congiuntivale, per mezzo dello scraping delicato della cornea, oppure con la raccolta di frustoli di tessuto in via di distacco. La metodologia dell’indagine diagnostica prevede l'isolamento del virus, mediante coltura su cellule permissive, o la sua identificazione nel campione prelevato dalla sede di lesione, con l’impiego di metodi diretti di colorazione, di immunofluorescenza o di ibridizzazione con DNA sonda. Nel caso in cui si voglia procedere all’isolamento, il prelievo va immediatamente posto in una provetta contenente terreno di trasporto, in modo da poter procedere all'insemensamento diretto sul monostrato di cellule permissive. Questo approccio metodologico presenta i vantaggi e gli svantaggi ben noti, per cui lo si utilizza solo se specificamente richiesto. La colorazione del preparato con la tecnica di Giemsa o di Papanicolau non consente di mettere in evidenza, con sufficiente certezza, le cellule giganti multinucleate e le inclusioni intranucleari patognomoniche; non può, pertanto. essere considerata una indagine affidabile. Riteniamo che per precisare con la rapidità e la affidabilità richieste dalla gravità della lesione, la diagnosi eziologica della cheratite erpetica e, più in generale delle cheratiti virali. è opportuno procedere all'identificazione del virus mediante immunofluorescenza diretta o mediante ibridizzazione con DNA probe specifici biotinilati. Esempi ben evidenti di immagini microscopiche patognomoniche sono già stati presentati nelle Figure 9 e 10 di pag. 44.
5.9 UVEITE
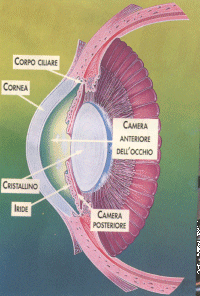
Con questo termine si designano le infezioni dell'uvea, che è composta da iride, corpo ciliare e coroide.L'iride costituisce la porzione anteriore del corpo ciliare, forma la pupilla e separa la camera anteriore da quella posteriore. Il corpo ciliare collega l'iride con la coroide, che è il rivestimento mediano dell'occhio, poiché è situata tra la sclera e la retina. La funzione dell'iride è quella di regolare la quantità di luce che penetra nell'occhio; quella del corpo ciliare di far variare la convessità del cristallino nell'accomodazione; quella della coroide di fornire supporto ematico e nutrizionale alla retina.Le uveiti possono avere differente eziopatogenesi ed interessare contemporaneamente e singolarmente tutte e tre le componenti uveali.
Si possono, quindi. classificare, ma non sempre distinguere sul piano eziopatogenetico e clinico, le uveiti anteriori (iriti ed iridocicliti), infettive e non infettive (allergiche) e le uveiti posteriori (corioretiniti). Le uveiti infettive, consistono in lesioni flogistiche di tipo essudativo e/o granulomatoso i cui agenti eziologici sono rappresentati da virus, batteri, miceti e protozoi. Insorgono, infatti, come complicanze, per via ematogena, nel corso di infezioni da virus della parotite, della rosolia, della varicella, possono rappresentare, meno frequentemente, particolari localizzazioni in corso di gonorrea, brucellosi e leptospirosi. Le uveiti posteriori riconoscono quali agenti eziologici Mycobacterium tuberculosis, MOTT, Toxoplasma gondii, Hystoplasrna capsulatum, Cryptococcus neoformans, Toxora canis. CMV. In ogni caso si impone la diagnosi eziologica, che non è facilmente eseguibile su prelievi diretti, ma può essere sospettata per la concomitante infezione sistemica oppure di altri organi ed apparati. La terapia, difatti, deve essere quanto più precoce e specifica possibile, al fine di evitare ulteriori complicanze oculari di una certa entità, quali retinite, cataratta e glaucoma.
5.10 ENDOFTALMITE
L’endoftalmite microbica rappresenta l’infezione di più grave prognosi e con gli effetti più invalidanti dell'apparato oculare. Per poter preservare la funzione visiva del malato sono richiesti non soltanto un corretto approccio clinico ma anche una diagnosi di laboratorio rapida, specifica ed affidabile. L’infezione endoftalmica può verificarsi per via endogena e per via esogena. La via endogena, od ematogena, si realizza per l'apporto ematico di microrganismi ai tessuti dell'occhio, in corso di setticemie. La via esogena si realizza in seguito ad interventi chirurgici intraoculari, a ferite oculari perforanti, a suppurazioni corneali complicate da fistole o da perforazioni. L’invasione diretta del globo oculare è una complicanza rara della cellulite orbitale da Mucorales. Cosi come nella cheratite microbica, l'eziologia risulta estremamente variabile, in relazione anche alle condizioni predisponenti ambientali e dell'ospite.
Endoftalmite esogena
Nei casi ad insorgenza più tipica, l'endoftalmite batterica esogena comincia entro 72 ore da un intervento chirurgico sull'occhio o da un trauma oculare di una certa gravità. È caratterizzata da diminuzione della visione,dolore, edema palpebrale, iperemia congiuntivale ed anche, chemosi, edema corneale e grave iridociclite associata ad ipopion. Gli agenti eziologici più frequenti nei casi postchirurgici sono S.aureus. S.epidermidis, St.pneumoniae, Proteus, Pseudomonas: nei casi post-traumatici l' eziologia è molto varia ed in quelli più gravi si riscontra Bacillus spp.(Bacillus cereus nel caso di endoftalmite al Policlinico Umberto I di Roma nel 1998 n.d.r.) L'insorgenza delle forme sostenute da bacilli non sporigeni è più tardiva; quella ad eziologia micotica può aver luogo dopo settimane o mesi dall'intervento, è caratterizzata da sintomatologia più subdola ed è causata da Aspergillus, Candida, Acremonium.
Endoftalmite endogena
Insorge nei soggetti con deficit immunitari, nei tossicodipendenti e nei soggetti con affezioni oculari di differente eziologia, trattati in modo improprio con terapia corticosteroidea locale. L'infezione è. quasi sempre bilaterale e si manifesta con diminuzione del visus ed iridociclite. Gli agenti eziologici possono essere S.aureus, Sr.pneumoniae, H.influenzae, N.meningitidis, M.fortuitum, Bacillus, Candida alhicans e meno frequentemente Aspergillus, Coccidioides immitis, Cryprococcus neoformans.
La diagnosi di laboratorio dell'endoftalmite infettiva richiede il prelievo del f1uido intraoculare sia di provenienza dalla camera anteriore che da quella posteriore. Il prelievo deve essere effettuato dal chirurgo in sala sterile, dalla zona di più estesa suppurazione, per aspirazione diretta oppure previa vitrectomia con l'ausilio di un microscopio operatorio. Il campione prelevato (0.2 ml di fluido della camera anteriore, 0.5 ml di vitreo) deve essere immediatamente inoculato nei terreni appropriati ed utilizzato per eseguire esami al microscopio. La colorazione di Gram permette una iniziale identificazione microbica; quella di Giemsa permette di differenziare, le componenti cellulari del fluido intraoculare, e di orientarsi verso altre affezioni quali uveiti e metastasi intraoculari. Il test al Limulus può essere di qualche utilità per mettere in evidenza la presenza. nel fluido prelevato di endotossine di batteri Gram negativi. Qualora, non fosse facilmente ottenibile il prelievo intraoculare è auspicabile, almeno inizialmente, effettuare prelievi congiuntivali e procedere come per le affezioni congiuntivali o corneali.
5.11 RETINITE
La retinite da Toxoplasma gondii è causata dal contagio per via ematogena, dalla moltiplicazione intraretinica e dall'incistamento del Toxoplasma. La lesione è caratterizzata da infiammazione essudativa della retina, vitrite ed iridociclite e da diminuzione monolaterale della visione. La diagnosi suggerita dalla anamnesi e dalla situazione obiettiva della retina può essere confermata in laboratorio mediante l’identificazione in fluorescenza diretta del Toxoplasma su adeguati prelievi intraoculari o, più semplicemente, mediante la determinazione del titolo anticorpale sierico con l'immunofluorescenza indiretta.
La retinite da Citomegalovirus può verificarsi quale complicanza della comparsa o della riattivazione dell’infezione virale in soggetti immunosoppressi o che hanno ricevuto un trapianto renale. La lesione è caratterizzata da infiammazione necrotizzante del tessuto retinico. La diagnosi è basata sui rilievi clinici e può essere confermata in laboratorio mediante l’identificazione diretta del virus, in immunofluorescenza o con ibridizzazione in situ con sonde biotinilate di DNA, nelle cellule dell’essudato flogistico e dell'epitelio corneale (Figura 16 di pag. 46) oltre che in quelle del sedimento urinario, del midollo osseo e nel buffy-coat del sangue (Figura 17 di pag. 46).
Nei giovani adulti, una retinite specifica è quella da Toxocara canis, causata dalla disseminazione intraretinica delle larve di questo parassita con conseguente flogosi granulomatosa e distacchi parziali della retina. La diagnosi di laboratorio necessita dell'aspirazione di f1uido intraoculare, su cui poter osservare la caratteristica eosinofilia, e di prelievi sierici adeguatamente distanziati nel tempo, per poter osservare l'incremento del titolo anticorpale specifico mediante il test in Elisa.
6
ALTERAZIONI DEL FILM LACRIMALE
Le lacrime hanno una peculiare composizione ed una modalità di secrezione, tali da poter compiere quattro funzioni: (i) lubrificare la cornea; (ii) contribuire al potere refrattivo dell’occhio, costituendo la superficie di contatto tra cornea ed aria; (iii) nutrire la cornea; (iv) svolgere un’azione antibatterica. La quantità di lacrime prodotta normalmente ad occhi aperti è di circa 0.8 microlitri/minuto, con alternanza di fasi rapide e fasi lente di produzione; la composizione chimica delle lacrime è riportata nella Tabella 8.
Tabella 8 - COMPOSIZIONE CHIMICA
DELLE LACRIME
| Na | 144-146 meq/L |
| K | 15-29 meq/L |
| Cl | 122-124 meq/L |
| HCO3 | 26 meq/L |
| Ca | 0.7-1.58 meq/L |
| Glucosio | 2.6-10 mg/100 ml |
| Proteine totali | 670-800 mg/100 ml |
| Albumina | 395 mg/100 ml |
| Globuline | 275 mg/100 ml |
| Ig G | 15 mg/100 ml |
| Ig A | 17 mg/100 ml |
| Ig M | 15 mg/100 ml |
| Ig D | 1 mg/100 ml |
| Ig E | 200 ng/100 ml |
| Acido ascorbico | 0.14 mg/100 ml |
| Lisozima | 70-200 mg/100 ml |
Il film lacrimale sulla superficie anteriore dell'occhio è mantenuto, quantitativamente e qualitativamente costante, grazie all'azione combinata della componente secretoria, costituita dalle ghiandole, dalla distribuzione, operata dall'ammiccamento delle palpebre, dalla escrezione che avviene attraverso le vie lacrimali. Il film lacrimale è composto da tre strati: esterno (lipidico), costituito da cere, acidi grassi e steroli, che riduce l'evaporazione della componente acquosa, intermedio (acquoso), interno, ad elevato contenuto di mucina. Il pH delle lacrime è la caratteristica chimica a cui sono legate la tolleranza delle lenti a contatto, la penetrazione tessutale di alcuni farmaci, l'azione fagocitaria nei confronti di batteri e corpi estranei.
Molte affezioni congiuntivali, e le eventuali complicanze corneali che possono derivarne, sono spesso legate a fattori che inficiano ed alterano la normale secrezione e composizione delle lacrime. Le alterazioni del film lacrimale (AFL) possono riconoscere vari e differenti meccanismi eziopatogenetici, riuniti nella Tabella 9.
Per quanto concerne la conferma in laboratorio della diagnosi di AFL, possono valere le indicazioni fornite dallo schema presentato nella Tabella 10. Nel caso della Sindrome di Sjogren, i criteri che rafforzano la diagnosi sono quelli che consentono di valutare la diminuzione del flusso lacrimale, la presenza di infiltrati linfocitari, la patogenesi autoimmunitaria. Ugualmente importanti sono i test diagnostici che confermano la diagnosi di altre affezioni che possono provocare AFL.
Situazioni correlate alla alterazione del film lacrimale
Sindrome di Sjorgen
Malattia di Steven-Johnson
Pemfigo oculare
Lupus eritematoso
Artrite reumatoide
Panarterite nodosa
Sindrome di Lyell
Sarcoidosi
Sindrome di Riley-Day
Ipovitaminosi A
Rosacea
Cirrosi biliare primitiva
Diabete mellito
Ipotiroidismo
Insufficienza estro-progestinica
Farmaci antidepressivi
Congiuntiviti croniche
Blefariti croniche
Lenti a contatto
Più in generale, i metodi diagnostici che consentono di valutare accuratamente la funzionalità lacrimale, rappresentati da indagini funzionali, da dosaggi dei componenti lacrimali e dalla valutazione della componente citologica. Tra i primi possiamo citare il Break-up-time che rappresenta il tempo intercorrente tra l'ultimo ammiccamento palpebrale e la comparsa delle zone asciutte sulla congiuntiva; il test di Schirmer che misura, invece, la secrezione lacrimale in condizioni basali e dopo stimolazione: infine i test di felcizzazione del muco lacrimale, vista la grande importanza della mucina tra i componenti delle lacrime.
---------------------------------------------------------------------------------------------------------------------
Tabella 10 – CRITERI DIAGNOSTICI DELLA S. DI SJOGREN.
E' una cheratocongiuntivite secca
Test di Schirmer (< 9 mm/5 min)
Test alla fluoresceina o al rosso bengala
Xerostomia:diminuzione del fluido salivare
Infiltrati leucocitari estesi all'esame bioptico delle ghiandole salivari
Test di laboratorio per malattia autoimmune
Debbono essere escluse contemporaneamente malattie quali: Linfomi, Graft versus host disease, AIDS, Sarcoidosi.
-----------------------------------------------------------------------------------------------------------------------
Tra i secondi, i test di misurazione del pH lacrimale; i tests di misurazione del contenuto di lattoferrina (immunodiffusione radiale) e di lisozima; i tests per la determinazione del contenuto di immunoglobuline e delle varie frazioni proteiche, che possono essere eseguiti sia mediante varie metodiche immunoenzimatiche, sia mediante il tracciato elettroforetico.
La valutazione della citologia congiuntivale può essere effettuata mediante scraping, oppure, molto più agevolmente e, con uguale efficacia in questi casi, per impressione mediante filtro di acetato di cellulosa. L’osservazione, dopo opportuna colorazione (Figura 18 di pag. 46), deve essere indirizzata alla valutazione della morfologia, della tintorialità e del rapporto nucleo/citoplasma delle cellule mucipare e di quelle epiteliali.
(16).
In conclusione, riteniamo di dover sottolineare come sia interesse reciproco dell'oftalmologo e del microbiologo clinico, ognuno per la propria sfera di competenza, giungere ad una attenta e critica standardizzazione delle procedure diagnostiche, di tutte le infezioni dell'occhio e degli annessi oculari. In particolare, al microbiologo clinico si richiede di mettere a punto tutte le metodologie di laboratorio più aggiornate che gli consentano di giungere ad una diagnosi eziologica ad elevato grado di specificità e sensibilità e di monitorare il trattamento chemioterapeutico, per quanto possibile, mirato.
(Da "Microbiologia clinica dell'apparato oculare" -Edizioni scientifiche Mascia Brunelli-Biolife di E. Gulletta)